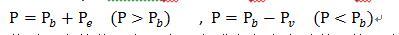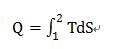|
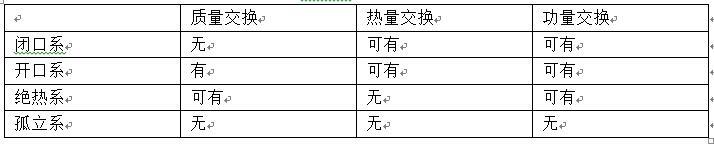
一、热力系统 1、(热力)系统: 系统:通常选取一定的工质或空间作为研究对象,称之为热力系统。 2、外界:与体系发生质、能交换的物系。 3、边界:系统与外界的分界面(线)。 边界可实可虚,可定可动。 二、系统的分类 根据系统和外界之间物质、能量的交换情况分: 1、闭口系统(控制质量):和外界没有物质交换。 2、开口系统(控制容积、控制体)和外界有物质交换。 3、绝热系统:和外界间没有热量交换。 4、 孤立系统:和外界既无能量交换又无物质交换。
三、平衡状态 (一)定义:无外界影响(重力场除外)的条件下,系统保持状态参数不随时间而改变的状态。 1、热平衡:在无外界作用的条件下,系统内部、系统与外界之间无温差。 2、力平衡:在无外界作用的条件下,系统内部、系统与外界之间无压差。 3、化学平衡:在无外界作用的条件下,系统内部、系统与外界之间无化学势差。 平衡的充要条件:系统同时达到热平衡、力平衡、化学平衡。 (二)平衡状态的特点: 1、在不受外界影响下,平衡不会自发的破坏; 2、处于不平衡的系统,在不受外界影响时,会自发的趋于平衡; 3、单相工质处于平衡状态时,在忽略重力的影响下,其内部性质均匀一致。 4、平衡必稳定,稳定未必平衡,平衡可以不均匀。 ★对于气液两相并存的热力平衡系统,气相和液相密度不同,所以整个系统不是均匀的。 四、状态参数 状态确定,状态参数的数值也确定,反之亦然。非平衡状态系统内部存在不平衡势,因此不能用状态参数来描写。 (一) 状态参数分类: 1、基本状态参数:压力P、比体积v、温度T(可以直接测量) 导出状态参数:内能U、焓H、熵S 2、强度参数:参数与系统质量无关,且不可相加。如:P、T 广延参数:参数与系统质量成正比,且可相加。如:m、V、U、H、S (二) 基本状态参数 1、 温度 摄氏温度 t(℃)与热力学温度T(K) 关系:t=T-273.15 2、压力(绝对压力)p Pa、MPa (压强)单位面积上的垂直作用力。 绝对压力p;表压力pe;真空度pv;环境压力pb。
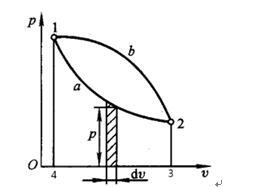
绝对压力的值不变,表压力或真空度会随着环境压力的变化而变化。 常用单位: 巴 1 bar =100000 Pa; 标准大气压 1 atm =101325 Pa; 工程大气压 1 at = 98066.5 Pa; 10米水柱的压力 毫米汞柱 1 mmHg =133.3224 Pa; 毫米水柱 1 mmH2O=9.80665 Pa。 注意:只有绝对压力 p 才是状态参数,才能直接进行热力计算。 3、比体积及密度 v = V/m =1/ρ m3/kg (三)简单可压缩系统(只有热量交换和体积变化功量的交换),只需两个独立的参数(如p、v,p、T 或v、T)便可确定它的平衡状态。 (四)状态参数坐标图 ①一简单可压缩系只需两个独立参数就可以确定其平衡状态 ②图上每一点都代表一个平衡状态。 ③ 不平衡态无法在坐标图上表示 五、功量 容积变化功的计算: 功是过程量,可以用p-v图上过程线与v轴包围的面积表示 功的符号约定:系统对外作功(膨胀)为“+”,W>0 外界对系统作功(压缩)为“-”,W<0 功和功率的单位:J或KJ,W或KW 示功图:
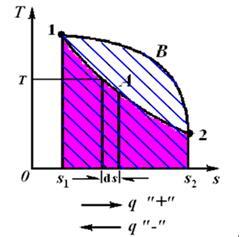
六、热量 定义:仅仅由于温差而通过边界传递的能量。 计算式
符号约定:系统吸热“+”,系统放热“—” ds>0:吸热; ds<0:放热; ds=0:绝热 单位:J或KJ 热量也是过程量,示热图
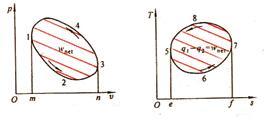
功与热量的异同: 1、均为通过边界传递的能量; 2、均为过程量; 3、功传递由压力差推动,比体积变化是作功标志; 热量传递由温差推动,比熵变化是传热的标志; 4、功是系统与外界之间,在力的推动下,通过宏观有序运动而传递的能量; 热是系统与外界之间,在温度的推动下,通过微观无序运动而传递的能量; 功转化为热是无条件的;热转化为功是有条件、限度的。 七、热力过程和热力循环 热力循环分类: 1、按性质分:可逆循环;不可逆循 2、按目的分:正向循环;逆向循环 (一)正向循环(动力循环)特点: 1、输出净功; 2、在p-v图及T-s图上顺时针进行; 3、从高温热源吸热,向低温热源放热,同时向外输出功。
(二)逆向循环特点:(制冷循环、热泵循环) 1、输入净功; 2、在p-v图及T-s图上逆时针进行; 3、从低温热源吸热,向高温热源放热,并消耗功量。
(三)循环经济性评价指标:
八、准静态过程、可逆过程与不可逆过程 (一)准静态定义:所经历的每一个状态都无限地接近平衡状态的过程。可以看成有一系列平衡态组成。 准静态实现条件: 1、在系统内外的不平衡势(如压力差、温度差等)较小。 2、过程进行缓慢、弛豫时间非常短。 3、工质有恢复平衡能力。 (二)可逆过程 定义:系统经历某一过程后,经原途径返回原来状态,使系统与外界同时恢复到初始状态,而不留下任何痕迹的过程,没有耗散效应的准静态过程。 可逆过程与准静态过程的关系: 1、可逆过程与准静态过程的差别就是有无耗散效应。 2、准静态过程是实际过程理想化,可逆过程是绝对理想的过程 3、可逆过程一定是准静态过程,准静态过程不一定是可逆过程。 (三)注意点: 1、可逆=准静态+没有耗散效应。 2、准静态着眼于系统内部平衡,可逆着眼于系统内部及系统与外界作用的总效果。 3、一切实际过程不可逆。 4、可逆过程可用状态参数图上实线表示 。 |
欢迎京津冀各位有志之士加盟天津优创科技空气能村村通私域独家代理,零投入,长久高回报,兼职创业首选!
加盟优创科技,共享环保红利!